Лікування раку ендометрія і її ефективність
За останні 30 років відбулася значна еволюція методів лікування раку ендометрія (РЕ), особливо при його I стадії.
Історія методів лікування даної нозології сягає своїм корінням в минуле століття. Паралельно із загальним визнанням методу хірургічного визначення стадії предоперационная ЛТ як стандарт лікування втрачає свою роль.
хірургічне стадирование дозволяє ідентифікувати справжню ступінь поширеності онкологічного процесу, а отже, істинну стадію раку ендометрія (РЕ). На підставі результатів досліджень, в яких стадії визначали хірургічним методом, встановлено, що приблизно у 25% хворих з I клінічною стадією захворювання поширюється за межі матки, а у багатьох пацієнток з II клінічною стадією переходу процесу на шийку матки не спостерігається.
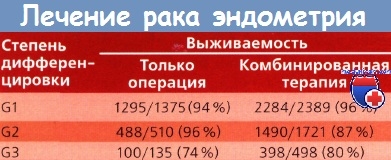
Пізніше було накопичено значну кількість даних про виникнення рецидивів в піхві і виживання хворих на рак ендометрія (РЕ) після хірургічного лікування і комбінованої терапії, що включає передопераційну брахітерапії і операцію. Крім того, проаналізовано дані про ступінь диференціювання пухлини і глибині інвазії в міометрій. Встановлено, що у хворих, які отримали перед- або післяопераційну ЛТ, частота рецидивів в області кукси піхви була нижче, хоча особливих відмінностей при високо- (G1) і помірно диференційованих (G2) пухлинах не виявлено.
Рецидиви в культі піхви не впливали на виживання. Показники виживаності після хірургічного лікування і комбінованої терапії (ЛТ + операція), особливо при помірно і високодиференційованих пухлинах, були однаковими. Виживання хворих з низкодиференційованими аденокарциномами після комбінованого лікування була дещо краща, ніж після хірургічного. Однак в більшості досліджень статистично значущі відмінності між цими групами пацієнток не виявлені.
Абдомінальної гістеректомію з двосторонньою аднексектомія проводять через 6 тижнів. Underwood і співавт. рекомендують виконувати екстирпацію матки відразу після завершення брахітерапії. При наявності глибокої інвазії в міометрій або метастазів застосовують ДЛТ в сумарній дозі 40-50 Гр на відповідні області. Underwood і співавт. показали, що глибину інвазії краще визначати шляхом вимірювання товщини міометрія, не порушеного пухлинним процесом, т. е. у напрямку від серозної оболонки всередину до межі пухлини. Якщо величина цього параметра менше 5 мм, ризик рецидиву високий, тому рекомендують проводити післяопераційну ДЛТ в сумарній дозі 40-50 Гр на область тазу.
При товщині неураженого міометрія від серозної оболонки більше 10 мм лікування може бути обмежена тільки хірургічним втручанням. Тактика лікування хворих з вільною від інвазії товщиною міометрія, вимірюваної від серози, рівній 5-10 мм, в даний час остаточно не визначена, хоча в цих випадках рецидиви виникають частіше, ніж при товщині цієї зони більше 10 мм.
Піхву було першим осередком рецидивирования захворювання тільки у 3,4% хворих, пацієнток з рецидивами в області тазу або віддаленими метастазами було в 4 рази більше. На думку Bond, післяопераційне опромінення піхви ефективно в невеликому відсотку випадків і не впливає на виживаність і частоту виникнення як рецидивів в області таза, так і віддалених метастазів незалежно від гістологічного типу пухлини. Тому він не рекомендує цей вид лікування в якості стандартної методики. Chen, виконавши невелике дослідження, що включило 32 хворих РЕ I стадії з глибокої інвазією в міометрій або низкодиференційованими аденокарциномами (G3), виявив, що в 18 випадках процес не виходив за межі матки. Нікому з цих 18 жінок післяопераційну ЛТ не проводили, і всі вони прожили більше 5 років.
У пацієнток з метастазами в лімфовузлах після хірургічного лікування спостерігався тривалий безрецидивний період. Однак більшість дослідників сьогодні виступають за застосування післяопераційної ЛТ у випадках метастатичного ураження лімфовузлів. Дані про поліпшення виживаності після ретельної лімфаденектоміі ще не представлені.

Kadar і співавт. ретроспективно провели аналіз лікування 262 хворих раком ендометрія (РЕ) з хірургічно встановленими стадіями. Ступінь диференціювання пухлини, глибина інвазії в міометрій, наявність пухлинних клітин в просвітах судин, перехід процесу на шийку матки, стадія РЕ за класифікацією FIGO і вік пацієнтки були незалежними прогностичними факторами. У хворих з наявністю одного несприятливого фактора або їх відсутністю ЛТ не впливала на відсоток виникнення рецидивів і загальну виживаність. Рівень 5-річної виживаності у цих жінок досягав 97%. На жаль, прогноз для більшості хворих з 3 або 4 несприятливими факторами ризику був поганим, незважаючи на проведену ЛТ. Напрошується питання, чи здатна ад'ювантна терапія поліпшити виживання, якщо 5-річний показник в цій групі хворих склав всього 17% за умови, що 5 з 6 пацієнток отримали ЛТ.
У наступній групі пацієнток, що мали два фактори ризику. 24 з 28 отримали ЛТ на область тазу з надією на поліпшення виживаності, проте статистично значимий результат досягнутий не був.
При порівнянні показників виживання і частоти виникнення рецидивів з урахуванням ступеня діфферен-цировки пухлини, а також інвазії в міометрій відмінності не виявлено. У хворих, які отримали ДЛТ, виявлено менше рецидивів в області таза, але більше віддалених рецидивів. У тих, хто не отримував ДЛТ, а тільки брахітерапії, кількість місцевих рецидивів було значно більше.
Creutzberg (Клінічне дослідження PORTEC, Нідерланди) ідентифікував 714 хворих з I стадією РЕ, у яких були високодиференційовані (G1) пухлини з інвазією в міометрій більше 50% його товщини, помірно диференційовані (G2) з будь-якою глибиною інвазії і низькодиференційовані (G3) з інвазією міометрія менше 50%. Хірургічне стадіювання не було обов'язковим критерієм включення в дослідження. Пацієнток рандомізовані в групу отримують післяопераційну ДЛТ або контрольну групу спостереження. Серед 654 хворих, які перебували під постійним наглядом, місцеві і регіонарні рецидиви зустрічалися рідше в групі ЛТ (4 vs 14%), ніж в групі контролю, а 5-річна виживаність була зіставною - 81 і 85% відповідно.
експерти GOG провели клінічне дослідження III фази, в якому порівнювалася ефективність хірургічного лікування з комбінованим (операція + ДЛТ на область тазу) у пацієнток з аденокарциномами ендометрія проміжного ризику. У дослідження були включені хворі з різною глибиною інвазії в міометрій, будь-яким ступенем диференціювання і без ознак метастазування в лімфовузли (стадії Ib, Ic, IIа і IIb). Всім проведено хірургічне стадіювання захворювання з гістологічним дослідженням лімфовузлів. До підгрупи високого ризику відносили:
1) пухлини G2-G3 з ураженням лімфатичних судин і зовнішньої третини міометрія,
2) вік 50 років або старше при наявності будь-яких двох перерахованих факторів,
3) вік більше 70 плюс будь-який з перерахованих вище факторів.

Всі інші хворі були віднесені до підгрупи низького ризику. ЛТ не призначили 202 жінкам, 190 отримали ДЛТ на область тазу. Середня тривалість спостереження становила 69 міс. У підсумку в групі не отримували ДЛТ рецидиви спостерігалися в 15,3% випадків у порівнянні з 6-8% в групі пацієнток, що піддалися опроміненню (р = 0,007). Місцеві рецидиви виявлені в 8,9 і 1,6% випадків відповідно. Загальне виживання через 48 міс. становила 86 і 92% відповідно, при чиною смерті в 50% випадків і більше в обох групах були супутні захворювання. Летальні результати, обумовлені основним захворюванням, становили 8,4 і 7,9% в групі не отримували і отримували ДЛТ.
Побічні ускладнення III і IV ступеня склали 4,9 і 14% відповідно. З 13 жінок з групи не отримували ДЛТ, у яких з'явилися рецидиви в області піхви, 12 призначили ЛТ, з них 5 померли внаслідок прогресування захворювання.
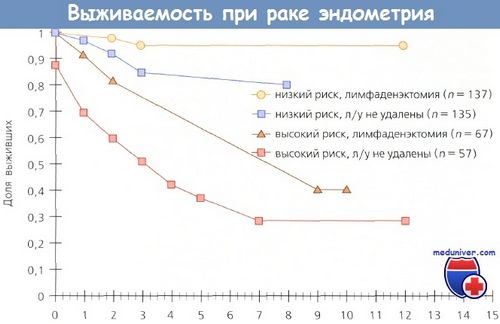
У таблиці представлені результати досліджень ефективності післяопераційної ЛТ при ранніх стадіях РЕ.
У 2/3 пацієнток були високодиференційовані аденокарциноми, у 41% - була відсутня інвазія в міометрій. У багатьох з цих хворих перед операцією ні встановлено діагноз гіперплазії ендометрія або РЕ. Ці факти представляють часту проблему всіх досліджень, в яких в якості хірургічного методу лікування при РЕ використовували влагалищную гістеректомію.
- Повернутися в зміст розділу "Онкологія"